囊胚移植后1到14天变化图 试管过程要小心
囊胚移植是将体外培养至第5-6天的胚胎植入母体子宫的过程,其后14天内将经历定位、黏附、侵入子宫内膜等关键阶段。从细胞分子层面看,这期间发生滋养层细胞分化、激素信号传递、母胎界面血管重构等精密调控,最终决定妊娠是否成功。整个过程如同精密编排的生物程序,母体通常无明显体感,但微观层面的变化已悄然完成。
移植初期的定位适应(第1-3天)
刚进入宫腔的囊胚仍包裹在透明带内,借子宫蠕动波和宫腔液流动寻找合适着床点。滋养层细胞开始分泌蛋白酶溶解透明带,完成"孵化"释放胚胎本体。此时子宫内膜处于窗口期,表面糖蛋白分子与胚胎表面受体相互识别。临床数据显示,约30%的囊胚在此期间因定位偏差或质量缺陷停止发育,属于自然淘汰机制。
黏附与初期着床(第4-6天)
囊胚滋养层外层细胞分化为合体滋养层,通过整合素家族蛋白锚定在内膜上皮。这一阶段类似生物胶水的黏附过程,胚胎会轻微侵入子宫内膜表层约0.1mm。母体基底膜释放肝素结合表皮生长因子(HB-EGF),促进胚胎-内膜信息交换。此时部分女性可能出现少量淡粉色分泌物,实为着床区毛细血管微量渗血,无需特殊处理。
绒毛膜成形与激素启动(第7-9天)
合体滋养层细胞形成树根状突起,分化为初级绒毛结构,开始建立原始胎盘循环。这些细胞同步分泌人绒毛膜促性腺激素(hCG),浓度以每48小时翻倍的速度增长。hCG刺激卵巢黄体持续分泌孕酮,维持子宫内膜蜕膜化。血液检测可在此时测出hCG>5mIU/ml,但尿检试纸灵敏度不足可能显示假阴性。
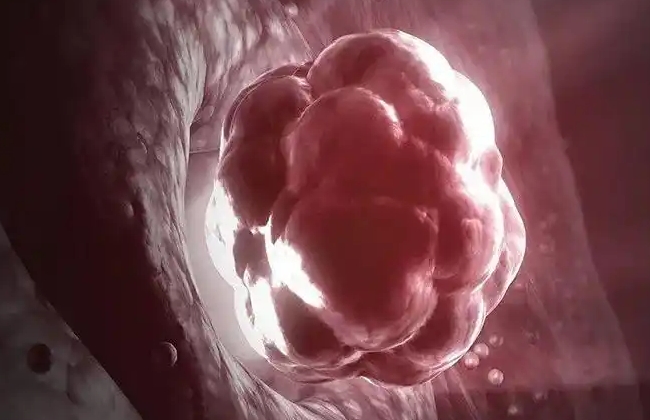
母胎界面血管重构(第10-12天)
滋养层细胞侵入子宫螺旋动脉,重塑血管结构使其失去收缩功能,确保胎盘血流供应稳定。这一过程伴随局部免疫调节,母体NK细胞分泌转化生长因子-β(TGF-β)抑制排斥反应。此时子宫内膜厚度可达12-14mm,形成富含糖原的蜕膜组织。部分敏感体质者可能感到乳房胀痛或轻微腹部拉扯感,与激素水平剧烈波动相关。
临床妊娠确认期(第13-14天)
血清hCG浓度通常突破100mIU/ml,胚胎完成初步器官原基分化。经阴道超声虽暂不可见孕囊,但生化妊娠已然确立。此阶段需警惕异位妊娠风险,若hCG增长缓慢或伴随腹痛需及时排查。医生会根据激素水平调整黄体支持方案,建议保持正常活动避免剧烈运动。
囊胚移植后的生理进程存在个体差异,约20%的妊娠在此时尚未达到可检测水平。建议移植14天后进行静脉血hCG检测,避免过早使用试纸引发焦虑。整个过程如同精密编排的生命序曲,既需要医学监测护航,也需要保持适度松弛的心态。生命的萌芽向来遵循其内在节律,耐心等待往往是最好的配合。
讨论群
与本文相关问答
大家一起在讨论
相关百科
最新百科
热门百科
- 试管胚胎移植后1-14天hcg标准值对照表,正常与否自己看
- 三级胚胎养囊成功率高吗?后续处理的优化策略
- 尿促性素打几天卵泡成熟?治疗终止的医学标准
- 囊胚移植后1到14天变化图 试管过程要小心
- 试管婴儿报销政策深度解读:2025年医保能帮你省多少钱?
- 人粒细胞刺激因子:试管移植中的内膜营养师与免疫调解
- 天津试管婴儿服务现状与未来趋势分析:技术突破背后的民生温度
- 冻囊胚移植后大忌 饮食生活都要讲究